ثقافة صحية
آفَتـان في مرض السكّـر (النوع الثاني) فرط الإنسـولين والهيموغلوبيـن المتسـكِّـر
![]() مقدمـة قصيرة: عـرّفت هيـئة خبراء مرض السـكـَّر في منظمة الصحة العالمية WHO مرض السكر بأنَّـه (حال مـزمنـة لارتفاع تركيز السكر في الدم نتيجة ظروف بيئية وعوامل وراثية تتفـاعل معـاً). إنَّ ارتفاع سكر الدم يعود إلى خلل في إفراز الإنسـولين، عدم فعاليـتها (تشمل مقاومة الخلايا لها) أو كليـهمـا. واختلال التوازن هذا يـؤدي إلى اضطراب في تمثيل (أيض) النشويات/السكريات، الشحوم والبروتينـات. كما أنّ التأثيرات الكبرى لمرض السكر تتضمن تلف أجهزة الجسم واضطراب وظائـفها وفشلـها بعد ذلك. لذا فإنّ ثمـّة شيـئـين في مرض السكر، السكر والإنسولين وعدم التوازن بينهما. الحديث هنا يتعلق بالنوع 2 من مرض السكر، حيث النوع 1 منه – المسمى (خطأ) بالطفولي - هو عدم وجود الإنسولين أو القليل منها. يكون التوازن عادة بإفراز كمية كافية من الإنسولين لـ (دفع) السكر الموجود في الدم والناتج عن تنـاول طعام غنيّ بالسكريات/ النشويات، إلى الخلايا لـ (حرقـه) والاسـتفادة منه في وظائـفها وفعـّالـيّـاتها المتعددة، وإبقاء السكر في الدم بتركير طبيعـي.
مقدمـة قصيرة: عـرّفت هيـئة خبراء مرض السـكـَّر في منظمة الصحة العالمية WHO مرض السكر بأنَّـه (حال مـزمنـة لارتفاع تركيز السكر في الدم نتيجة ظروف بيئية وعوامل وراثية تتفـاعل معـاً). إنَّ ارتفاع سكر الدم يعود إلى خلل في إفراز الإنسـولين، عدم فعاليـتها (تشمل مقاومة الخلايا لها) أو كليـهمـا. واختلال التوازن هذا يـؤدي إلى اضطراب في تمثيل (أيض) النشويات/السكريات، الشحوم والبروتينـات. كما أنّ التأثيرات الكبرى لمرض السكر تتضمن تلف أجهزة الجسم واضطراب وظائـفها وفشلـها بعد ذلك. لذا فإنّ ثمـّة شيـئـين في مرض السكر، السكر والإنسولين وعدم التوازن بينهما. الحديث هنا يتعلق بالنوع 2 من مرض السكر، حيث النوع 1 منه – المسمى (خطأ) بالطفولي - هو عدم وجود الإنسولين أو القليل منها. يكون التوازن عادة بإفراز كمية كافية من الإنسولين لـ (دفع) السكر الموجود في الدم والناتج عن تنـاول طعام غنيّ بالسكريات/ النشويات، إلى الخلايا لـ (حرقـه) والاسـتفادة منه في وظائـفها وفعـّالـيّـاتها المتعددة، وإبقاء السكر في الدم بتركير طبيعـي.
تفرز غـدّة البنكرياس التي تحتوي على ملـيـون جزيرة تقـريباً من جزر لانغرهانز عدة هورمونات حسب مجموعات خلاياهـا، وهي:
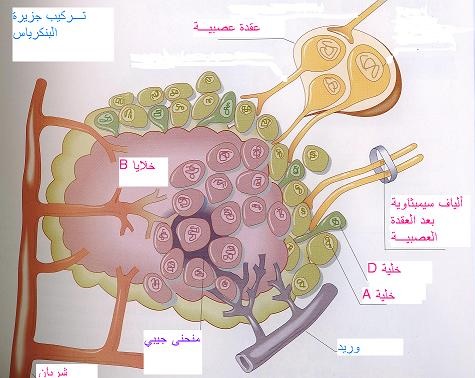
1. خلايا ألفا (A) التي تنتج هورمون كلوكاكون Glucagon.
2. خلايا دي (D) التي تنتج هورمون سوماتوساتين Somatostatin.
3. وخلايا بيتا (B) وتنتج الإنسولين.
تتفاعل هذه الخلايا فيما بينها مباشرة أو خلال تماسِّ إفرازاتـها. فمثلاً، يحفـّز الكلوكاكون إفراز الإنسولين، بينما يثـبِّـط السوماتوستاتين إفرازاتهما، حسب ظروف الفرد. تسير العملية بصورة طبيعية إذا كان الفرد سليما معـافى. تبدأ العملية بعد دخول السكر إلى الدم، حيث يحفز الكلوكوز إطلاق الإنسولين بدخوله خلايا بيتا التي تستعمله قبل أن تطلق الإنسولين إلى الدم التي يظهر مفعولها الحيوي بارتباطها بمستقبـِلات (بكسر الباء الثانية)، وهي بروتينات موجودة على سطح الخلية. وبعد هذا الارتباط (المستقبـِل-الإنسولين) تنفتح الخلية لدخول الكلوكوز.
أما إذا كانت المستقبلات ذات خلل يمنع الارتباط، أو عجزت الخلية عن (إعطاء) إشارة إلى الكلوكوز لدخولها بعد الارتباط، يتصاعد تركيز السكر في الدم وتتصاعد معه الإنسولين. ومن هنا يحدث الخطر إذا لم يتدارك الشخص أمره قبل فوات الأوان فيحصل على مرض السكـر.
فـرط الإنسـولين Hyperinsulinemia
عندما تكون هناك مقاومة، تقل كمية الكلوكوز الداخلة إلى الخلية، وتزداد في الدم. هذه الزيادة تضغط على البنكرياس لتضـخّ إنسولين أكثر كتعويض عن عدم فعاليتها أو جدواها، وباستمرار هذا الضغط والضخ، تستهلك البنكرياس وتستنفد الإنسولين فيها أو تقل، فيكون الاعتماد على الإنسولين (الخارجية) ضرورة لازمة للتعويض عما فـُقـِد. ومن هنا يمكننا تعريف المقاومة بأنها الحال التي لا تستطيع الإنسولين فيها أنْ تـُظهـر مفعولها في تخفيض سكر الدم فيزداد إفرازها تعزيزاً لفعلها. ففي الشخص الطبيعي مثلاً، تكفي (وحدة) من الإنسولين لإدخال 10 ملغم من الكلوكوز إلى الخلايا. ولكن في حال فرط الإنسولين نحتاج إلى 10 وحدات لإدخال هذه المليغرامات العشرة من الكلوكوز إلى الخلايا. لا تمنع الإنسولين تحرّرَ الشحوم من الخلايا وحسب، بل وتسبب تراكم الشحوم فيها، وتجعل الشخص جائعاً، فيلجأ إلى الطعام وقد يُـفرط فيه فيسمن. فبينما تنقذ الإنسولين حياة المصاب بالنوع (1) من مرض السكر، تكون كارثة على بعض مرضى النوع (2)، وخصوصاً المسنين منهم، فيزداد وزنهم وتزداد أمراضهم. ألا إنَّ فرط الإنسولين في الدم ليس نذيراً بوقوع مرض السكر. فهناك، رغم اختلاف آراء الباحثين، شخص واحد من كل أربعة أشخاص ذوي مستوى إنسولين عال، يصاب بالسكر. كما أنّ فرط الإنسولين في الدم يرجع إلى أمراض أو حالات أخرى. فمثلاً، إنَّ تكوّنَ الحصى المستمر في الكلية يسبب فرط الإنسولين، كما أنَّ المرأة التي تعاني من مرض المبيض متعدد الأكياس Polycystic Ovary Disease قد يكون لديها فرط الإنسولين. ومن هنا يمكن القول إنه ليس كل من لديه فرط إنسولين يصاب بمرض السكر، ولكنْ كلّ مريض سكر لديه فرط إنسولين. ورغم وجود هذه الكمية الكبيرة من الإنسولين في الدم، يبقى تركيز السكر في الدم عالياً مما حيّـر الباحثين. ربما يعود هذا إلى مقاومة الخلايا الناتجة عن فرط الإنسولين، لأنّ هذه الإنسولين المتزايدة تغطـّي/تغسل مستقبـِلات الإنسولين الحساسة الواقعة على سطح الخلية فتفقدها حساسيتها. لذا يكون الاعتدال في تناول مثل هذه الأطعمة أمراً لازماً لتفادي الإفراط. إنّ زيادة الإنسولين في الدم تكون السبب في استلام بعض الأنسجة نسبة كبيرة من الإنسولين التي لا تحتاجها، فتسبب تلفها، كالكلية مثلاً التي يكون احتمال تلفها 17 مرة أكثر من الحال الطبيعية.
أما علامات فرط الإنسولين فهي زيادة محيط الخصر عن محيط الحوض، رغبة في التهام السكر، شعور بالنوم بعد وجبات الطعام، أرق في الليل يذهب بتناول بعض الطعام وسمنة في البطن التي تكون كالتفاحة شكلاً. وهنا تزيد الشحوم الثلاثية ويقل الكوليستيرول الجيد، بينما لا يتأثر الكوليستيرول الضار ويرتفع ضغط الدم.
العوامل الوراثيـة
إذا كان في العائلة تأريخ ارتفاع ضغط الدم، سكتة قلبية، السكر(النوع الثاني)، فهناك احتمال قوي بأن لدى الشخص فرط الإنسولين. ويظهر أنَّ ثمة خمسين في المائة للوراثة وخمسين في المائة لنوع الحياة التي يحياها. وهذا الأخيرة تتضمن 50% بدانة و50% عدم مزاولة الرياضة. إنّ بعض الأشخاص يولد بخلل وراثي يجعل أجسامهم تفرط في إفراز الإنسولين عندما يتناولون الكاربوهيدرات / السكريات.
وقد أوضح جيمس بلاند عام 2000 أنّ فرط الإنسولين هو متعدد الجينات وليس جيناً واحداً. وقد دلت الأبحاث أنّ ضَعفَ خلايا بيتا تزيد من إنتاج السكر في الكبد وتقلل من حساسية الإنسولين الكاتب. الطرفية وهي اضطرابات جينية. وحسب قـول بلاند (المحيط قابل للتغيير وأما الجينات فلا.)
وعلى هذا الأساس فإنَّ استعمال بعض الأدوية من عائلة سلفونيل يوريا، مثل كلايبيورايد (Diabeta - micronase) وغيرها من الأدوية التي تحفز البنكرياس على الإفراز، في تخفيض مستوى سكر الدم، يسبب فرط الإنسولين ويؤدي إلى استهلاك البنكرياس على المدى البعيد، مما يستوجب زرق الإنسولين. ربما يكون استعمال ميتفورمين Metformin ( كلوكوفاج Glucophage ) خير بديل. إذ أنَّـه، بالإضافة إلى تثبيطه إطلاق/تحرير السكر من الكبد، يخفض الوزن أيضاً.
إنَّ بعض الأدوية التي تستعمل في معالجة ضغط الدم العالي والمواد المدرّرة والمهدئات النفسية وسلفونيل يوريا تزيد من المقاومة للإنسولين.
ويبقى العلاج الفعال لهذه الحال هو تخفيض الوزن، بتناول طعام معتدل بكمية محدودة وممارسة التمارين الرياضية.
الهيموغلوبين المتسـكـّر
في مجرى الدم توجد خلايا الدم الحمر وهي متكونة من مواد كيمياوية. تحتاج هذه الخلايا، كباقي خلايا الجسم، إلى السكر كطاقة، للقيام بوظيفتها. تلتصق بعض جزيئات السكر (الكلوكوز) بالهيموغلوبين الموجود فيها فيتكون ما يسمّى بالهيموغلوبين المتسكر (Glycated or glycosylated Haemoglobin)، ويرمز له اختصارا HbA1c)). وكلما ازداد تركيز الكلوكوز، ازدادت نسبة هذا الهيموغلوبين. وإنّ الغرض من فحصه مختبرياً هو لقياس عدد جزيئات الكلوكوز الملتصقة بالهيموغلوبين، التي تـُفصح بدورها عن معدل تركيز الكلوكوز في الدم خلال فترة الشهرين إلى الثلاثة شهور الماضية.
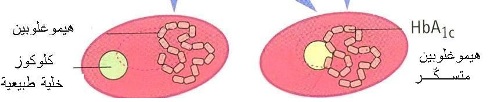
النسبة العادية (الطبيعية) للإلتصاق هي 4% إلى 6% في الشخص السليم من مرض السكر. أما في مريض السكر، فقد تكون النسبة التي لا تتجاوز 7% جيدة أيضاً. أما إذا كانت 8%، وجب اتخاذ الإجراء اللازم لتخفيضها. أما إذا تجاوزت 8%، فهذا يعني أن المريض أصبح عرضة لأمراض العين والكلى وتلف الأعصاب وغيرها، فعليه اتخاذ إجراءات فورية لتخفيضها.
التخلص من الهيموغلوبين المتسـكـِّر
من حسن الحظ أنَّ عمر خلايا الدم الحمر أربعة أشهر، وهذا يعني أنَّ الهيموغلوبين المتسكّر يذهب معها خلال هذه المدة، فتتولد خلايا جديدة يكون باستطاعة المريض تقليل الهيموغلوبين المتسكّر فيها بالسيطرة على تركيز كلوكوز الدم، وذلك بتناول طعام يحتوي على كميات قليلة من الكاربوهيدرات/السكريات مصحوباً بتمارين بدنية منتظمة وأدوية إن اقتضى الأمر. وعندما يكون تركيز كلوكوز الدم طبيعياً أو أقرب إلى الطبيعي، يكون الهيموغلوبين المتسكر بنسبة جيدة تبعد التأثيرات الخطرة عن الجسم. يتغير تركيز السكر في الدم من ساعة لأخرى ومن يوم ليوم، لذا يعتبر مستوى السكر في الدم خير دليل على المرض. أما الهيموغلوبين المتسكر، فيتغير ببطء خلال عشرة أسابيع، لذا يكون (مقياساً) للسيطرة على مرض السكر. وهذا يعني أنه إذا كان تركيز السكر صباحاً قبل الفطور في حال طبيعية 3.8-6.1 مليمول/ ل، فهذا جيد، ولا يسبب نسبة عالية من الهيموغلوبين المتسكر. ولكن السكر الناتج بعد وجبات الطعام Postprandial يلعب الدور الكبير. ففي هذه الحال يجب ألاّ يزيد تركيز سكر الدم عن 11.1 مليمول/ل (200 ملغم/دل) بعد ساعتين من تناول الطعام. (ولكنّ التركيز الذي لا يزيد عن 8 ملمول/ل أو 144 ملغم/دل هو المرغوب حاليّاً لدى جمعية مرض السكر الأمريكية – إضافة من الكاتب) أما تركيزه عند النوم فـيُستحسن أن يكون بين 4.5 – 6.7 مليمول/ل. وقد يكون التركيز (8 مليمول/ل = 144 ملغم/دل) مقبولاً.
وخلاصة القول إنّ السيطرة على تركيز سكر الدم بجعله في مستوى طبيعي، ويتم هذا بتخفيض الوزن، بتناول غذاء متوازن بكميات معينة في أوقات محددة، وبممارسة التمارين الرياضية المنتظمة، تبقى الطريق الوحيد للتخلص من مرض السكر أو جعله تحت السيطرة الدائمة لتفادي الأمراض المهلكة الناجمة عنه.
بهجت عباس
.............................
من كتاب (الجينات والعنف والأمراض – فيشون ميديا – السويد 2007)
ملحق
وهنا أحبّ أن أضيف بعض المعلومات عن آلية ازدياد الوزن (السمنة) في مريض السكر نوع 2 التي يمكن تلخيصها بعمليّتين اثنتيْن:
1. تكوّنُ الشحوم Lipogenesis - تحويل سكّر الدم إلى شحم (دهن) حيث يتمّ تراكمه وخزنه في الأنسجة الشحمية.
2. تحلّلُ الشحوم Lipolysis - عملية تفكّك / تحلّل الشحوم لإنتاج طاقة.
تسيطر على هاتين العمليتين هورمونات تُفرز من البنكرياس والغدة النخامية pituitary gland والغدة الكُظريّـة adrenal gland التي تفرز الأدرينالين.
تثّبط الانسولين إفراز الكلوكاكون وبهذا لا تتمّ عمليّة تحلل الشحوم.
في مرض السكر –النوع الثاني- يقاوم الجسم الإنسولين فتحاول البنكرياس التعويض بإفراز أكثر، وبهذا يكثر تخزين الشحوم الثلاثيّة triglycerides في الخلايا الشحمية. فعمل الإنسولين هو تحفّيز إفراز إنزايم لايبيس Lipase في الخلايا الشحمية، هذه الإنزايم تأخذ الحوامض الشحمية إلى الأنسجة لتحولّها إلى شحوم ثلاثية فتُخزن. لكنّ الإنسولين التي تحفّز إفراز اللايبيس من الخلايا الشحمية تثّبط (تمنع) إفراز اللايبيس من الخلايا العضلية، لذا لا تتحرر الحوامض الشحمية لتكون مصدر الطاقة بدلاً من السكّر
ولكنْ عندما بحتاج الجسم إلى طاقة ويكون مستوى سكر الدم واطئاً غير كافٍ لتزويد الجسم بالطاقة، ينشط إفراز الكلوكاكون والأدرينالين بدلاً من الإنسولين، وهذان يحطّمان أو يفكّكان الشحوم الثلاثية المخزونة في الأنسجة الشحمية، فتنتج الحوامض الشحمية والكليسرول فتكون مصدراً للطاقة. لذا عدم تناول السكّريات يؤّدي إلى عدم إفراز الإنسولين من ناحية وإلى استعمال الشحوم مصدراً للطاقة من ناحية أخرى فيفقد الجسم من وزنه.
وفي هذه الحال، يعني قلة السكر في الدم، يلعب الكلوكاكون دوره بدلاً من الإنسولين، وهنا يأتي دوره بتحفيز الخلايا العضلية لفرز اللايبيس التي تفكِّكك (تجزّئ) الشحوم إلى حوامض شحمية لتكون مصدراً للطاقة.








